BRASÍLIA- A Agência Nacional de Vigilância Sanitária (Anvisa) divulgou na noite de sexta-feira, 17, sua proposta para reforçar as regras de importação e manipulação de insumos para canetas para obesidade.
Entre vários pontos, a Anvisa quer exigir que as empresas atendam a critérios de qualidade para importação do ingrediente farmacêutico ativo (IFA), apresentando, por exemplo, o certificado de Boas Práticas de Fabricação (CBPF) de onde o insumo foi produzido. Outro tópico trazido pela regra é a criação de um sistema de vigilância para que farmácias de manipulação notifiquem eventos adversos ocorridos após o uso de canetas manipuladas.
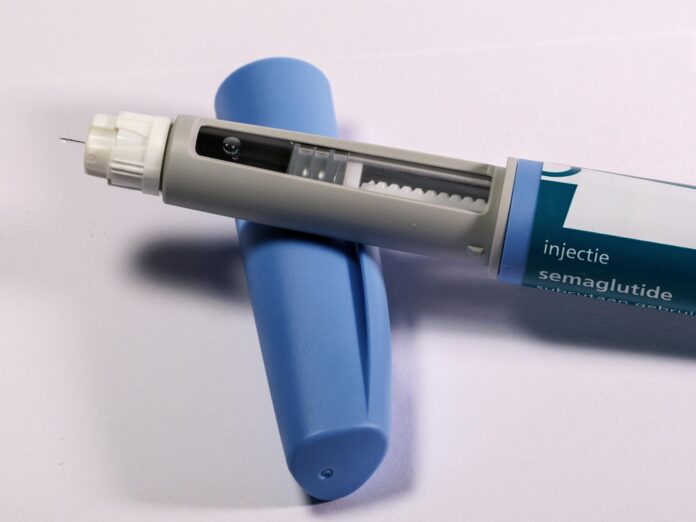
Anvisa identificou que a tirzepatida tem sido manipulada indiscriminadamente, sendo que processo é autorizado em casos específicos. Também há problemas de importação de medicamentos sem registro no Brasil ou falsificados Foto: millaf (Nemchinova)/Adobe Stock
A minuta disponibilizada pela agência em seu site é o primeiro passo dessa reformulação e será votada no dia 29 de abril pela diretoria colegiada do órgão. Após a aprovação do texto, as empresas terão um prazo de 120 dias para se adequar. No período de transição, as importações deverão ser previamente aprovadas pela agência por meio de pedido de liberação.
A Anvisa decidiu endurecer as regras para importação e manipulação de insumos para canetas após fazer um dossiê dos problemas verificados no País em decorrência da ampliação da comercialização desses medicamentos. A Anvisa identificou os seguintes riscos:
- Problemas de esterilização e consequente risco de contaminação biológica;
- Falhas na cadeia de armazenamento e transporte;
- Ausência de controle adequado de cadeia fria e condições ambientais;
- Uso de insumos irregulares, sem controle de qualidade e de origem desconhecida.
Atualmente, no Brasil, é permitida a manipulação da tirzepatida (princípio ativo do Mounjaro) para casos específicos. Porém, a Anvisa identificou que o produto tem sido manipulado indiscriminadamente. Entre novembro de 2025 e abril, foram importados mais de 100 quilos de IFA de tirzepatida, o suficiente para produzir cerca de 20 milhões de canetas de 5 mg.
Além disso, a agência verificou problemas na importação de medicamentos para obesidade sem registro no Brasil ou falsificados. Diante do cenário, o órgão anunciou no início do mês a revisão das normas de fiscalização.
Certificados
Um dos principais pontos que a Anvisa quer exigir é a comprovação de que a produção dos insumos que entram no Brasil para produção de canetas, sobretudo manipuladas, segue padrão de qualidade da agência. Nesse sentido, passará a exigir uma série de documentos.
Um dos principais é o Certificado de Boas Práticas de Fabricação. O documento prova que o local onde ocorre a produção do ingrediente farmacêutico ativo (IFA) usado no medicamento segue parâmetros rigorosos de qualidade, atestados pela Anvisa.
Atualmente, esse documento não é exigido, de modo que a agência não consegue garantir a qualidade do local onde o insumo é produzido. A exigência do CBPF já ocorre, por exemplo, no caso da produção de vacinas.
A proposta ainda prevê a necessidade de apresentar a Carta de Adequação do Dossiê de Insumo Farmacêutico Ativo (Cadifa). Esse documento serve para atestar que o IFA foi produzido seguindo testes de qualidade e segurança. Os fabricantes também podem apresentar como alternativa o Certificado de Adequação à Monografia da Farmacopeia Europeia (CEP), que é um documento semelhante emitido pela agência europeia.
Armazenamento
A minuta também dedica um capítulo para armazenamento e transporte dos IFAs. O texto determina que esses processos devem cumprir as exigências estabelecidas pela norma da agência que já está em vigor ou regra futura sobre o tema.
Entre as diretrizes desse regulamento está, por exemplo, a exigência de manter a temperatura adequada ao guardar os insumos. Isso é uma preocupação importante no caso de substâncias análogas ao hormônio GLP-1, que precisam ficar na geladeira, sob risco de perder a eficácia e segurança caso não sejam armazenadas adequadamente.
As empresas importadoras deverão comprovar que as condições de armazenamento e transporte estão de acordo com o exigido. As farmácias de manipulação também terão de justificar o prazo para uso do medicamento manipulado e suas condições de armazenamento.
Eventos adversos
A proposta publicada pela Anvisa determina que as farmácias de manipulação deverão estruturar um sistema de farmacovigilância, ou seja, uma estrutura para registrar suspeita de eventos adversos do uso de canetas para obesidade manipuladas e notificar a Anvisa.
No caso de eventos adversos que levem à morte, a Anvisa quer que as farmácias de manipulação façam a notificação, por meio do sistema eletrônico da agência, no prazo máximo de sete dias corridos.
Para as suspeitas de eventos adversos graves, mas que não resultem em óbito, a Anvisa fixa um prazo de 15 dias corridos para notificação.
“As farmácias de manipulação devem manter registros completos, rastreáveis, íntegros e auditáveis de todas as atividades de farmacovigilância realizadas, incluindo notificações, avaliações, comunicações e decisões, devendo tais registros permanecer disponíveis para inspeção pela autoridade sanitária”, diz a minuta.
Fonte: Estadão




